galleggiano in un bicchiere d’acqua, sciogliendosi, non
fanno sollevare ulteriormente il livello del liquido.
Si veda ache un’altra risposta a: http://www.vialattea.net/esperti/php/risposta.php?num=9708
Un blocco di ghiaccio, immerso
nell’acqua di un contenitore, ne aumenta il livello
poichè viene spostato un volume di acqua pari a quello
della porzione di ghiaccio immersa. Poichè il ghiaccio
ha una densità inferiore a quella dell’acqua liquida (a
0°C 0,9168 contro 0,9998, per questo galleggia) non
tutto il blocchetto è immerso ma una parte, pari a meno
di un decimo del volume totale, rimane al di fuori della
superficie (si pensi per esempio agli iceberg, la cui
parte emersa è “proverbialmente” molto minore
di quella sommersa). Man mano che il ghiaccio del
blocchetto si scioglie, il volume di acqua spostata
diminuisce e conseguentemente, il livello dell’acqua nel
bicchiere dovrebbe a sua volta abbassarsi. Tuttavia, ciò
non avviene, poiché l’acqua del ghiaccio fuso va
gradualmente ad aggiungersi all’acqua del bicchiere,
facendo in modo che, nel complesso, il livello dell’acqua
non diminuisca e non aumenti con il progressivo
scioglimento del ghiaccio.
Il comportamento dell’acqua nel passare
dallo stato liquido a quello solido è particolare, in
natura: contrariamente ad altre sostanze, infatti, al
diminuire della temperatura e precisamente poco prima del
congelamento, (per l’acqua distillata, ciò avviene a
0°C) aumenta il proprio volume (e la densità diminuisce
conseguentemente). Il comportamento anomalo ha luogo al
di sotto dei 4 gradi C (temperatura alla quale l’acqua ha
la sua massima densità, 1 g/cm3): al di sopra, con
l’abbassarsi della temperatura, il volume diminuisce come
negli altri liquidi.
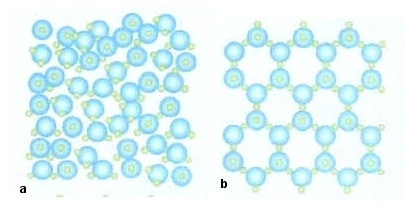 |
Dalla
figura si comprende benissimo che lo stesso numero di molecole
d’acqua cristallizzate (ghiaccio) occupa uno spazio maggiore rispetto
alla stessa quantità di molecole d’acqua liquida.
L’aumento di volume dell’acqua dopo il
passaggio allo stato solido è pari a circa il 9 per
cento del volume iniziale. La densità del ghiaccio è
cioè pari al 91,7% di quella dell’acqua liquida.
Quindi, se facessimo ghiacciare un litro d’acqua liquida (1 dm3=1000 cm3) otterremmo un blocco di ghiaccio dal volume di circa 1087 cm3.
Tale blocco potrebbe essere un parallelepipedo a base quadrata con lato
di 10 cm e con altezza di cm 10,87. Se messo in acqua, tale blocco
galleggerebbe emergendo dal livello dell’acqua per circa 9 millimetri.
Il fatto che una massa di ghiaccio
galleggiante, sciogliendosi, non aumenti il livello del
liquido nel quale è immersa è fondamentale nello studio
delle possibili evoluzioni climatiche del nostro pianeta.
Infatti, bisogna tenerne conto quando si cerca di stimare
il sollevamento del livello medio del mare, causato dal
riscaldamento globale (per effetto serra) e dal
conseguente scioglimento dei ghiacci. Infatti, l’aumento
del livello medio del mare, stimato in quasi un metro
entro la fine del prossimo secolo, sarà imputabile allo
scioglimento parziale dei ghiacci della Groenlandia e
dell’Antartide (i quali poggiano su isole o continenti –
ma soprattutto, si trovano al di fuori delle acque),
mentre i ghiacci dell’artico, essendo già galleggianti
(in effetti nel polo nord non esiste un continente come
in Antartide, ma c’è solo un mare profondo quasi
quattromila metri) non contribuiranno a questo aumento.