Gli aminoacidi, o amminoacidi, sono delle molecole organiche, cioè costituite da una catena di atomi di carbonio e sono caratterizzati dalla presenza costante di un gruppo funzionale acido (carbossilico, COOH) ed uno amminico (NH2), dai quali deriva il nome.
In natura esistono molti tipi di aminoacidi, e tra questi soltanto 20 vanno a costituire le proteine. Negli aminoacidi proteici, i due gruppi acido e amminico sono entrambi legati ad un carbonio chiamato α (alfa), per cui sono detti anche α-aminoacidi. A seconda di come gli altri carboni o gli altri gruppi chimici legati al carbonio alfa sono disposti nello spazio rispetto ai gruppi acido e aminico, si distinguono gli L-aminoacidi e i D-aminoacidi. Gli aminoacidi proteici sono tutti L-aminoacidi.
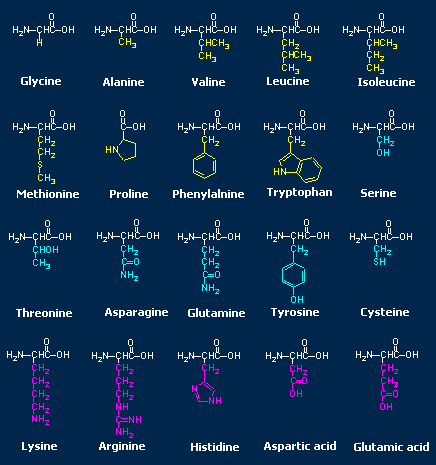
I 20 aminoacidi proteici. Nella figura sono evidenziate le catene laterali di ogni aminoacido.
Gli altri gruppi legati al carbonio α possono essere dei semplici idrogeni, ed allora si avrà l’aminoacido più semplice, la glicina. Oppure molecole cicliche, cioè una catena di carboni chiusa ad anello, come la prolina; gruppi alcolici (-OH) come nella serina o la treonina; gruppi contenenti zolfo come per esempio nella cisteina o nella metionina; gruppi azotati come nella glutammina o nell’arginina; gruppi carbossilici, acidi, come nell�aspartato; gruppi aromatici, cio� molecole cicliche con legami doppi tra i carboni, per esempio il triptofano; oppure catene di carboni ramificate. Queste ultime si trovano negli aminoacidi leucina, isoleucina e valina.
I gruppi laterali sono molto importanti perché danno all’aminoacido specifiche caratteristiche chimiche, e permettono la stabilizzazione della struttura tridimensionale della catena proteica attraverso attrazioni e repulsioni deboli. Infatti, gli amminoacidi sono legati tra di loro nella catena polipeptidica dal legame peptidico, covalente, tra il gruppo carbossilico e quello aminico. (In questo sito vedrete una animazione della sintesi del legame peptidico: http://biotech-adventure.okstate.edu/low/basics/protein/09-peptide_linkage/ ). La sequenza degli aminoacidi è la struttura primaria della proteina. La catena peptidica si ripiega poi in talune zone in strutture tridimensionali secondarie obbligate, spesso ripetitive, dovute alla struttura tridimensionale degli aminoacidi, come per esempio le alfa-eliche; e in strutture terziarie che sono un ulteriore ripiegamento dovuto sia all’ingombro sterico, cioè spaziale, delle catene laterali che alle attrazioni e repulsioni deboli, sia tra i gruppi laterali degli aminoacidi che tra essi e il mezzo in cui la catena proteica è immersa.
Gli aminoacidi ramificati, in particolare, sono molecole non polari, e quindi respingono l’acqua. La maggior parte delle proteine è immersa in un mezzo acquoso; ripiegandosi su se stesse, le proteine espongono all’esterno gli aminoacidi polari, che in contatto con il mezzo acquoso stabilizzano la conformazione proteica e mantengono all’interno del ripiegamento gli aminoacidi non polari. Le proteine immerse nelle membrane biologiche, invece, espongono gli aminoacidi non polari all’esterno del ripiegamento, nella porzione di proteina che sta immersa nella membrana, dato che l’interno delle membrane biologiche è non polare.
Oltre ad avere funzione plastica e funzionale nella costituzione di proteine strutturali ed enzimi, gli aminoacidi entrano anche nei processi cellulari di produzione dell’energia, soprattutto in condizioni di carenza di altre molecole di più pronta demolizione, come gli zuccheri. Circa il 5-10% dell’energia prodotta deriva dalla demolizione degli aminoacidi.
Dei 20 aminoacidi proteici, l’organismo non è in grado di sintetizzarne otto e deve quindi assumerli attraverso l’alimentazione. Essi sono quelli ramificati: valina, leucina, isoleucina e quelli non ramificati: alanina, prolina, fenilalanina, triptofano, metionina.
I risultati di alcune ricerche mostrano che nel muscolo gli aminoacidi ramificati vengono degradati durante l’esercizio fisico e l’attivazione dell’enzima, che ne regola l’ossidazione, dipende dall’intensità dell’esercizio. Ciò ha suggerito che un’integrazione alimentare con tali molecole possa fornire "carburante" al muscolo e quindi migliorare la resa atletica, evitando che gli aminoacidi necessari vengano"ottenuti" dalla degradazione delle proteine muscolari. Tuttavia, altri studi hanno evidenziato che la somministrazione di tali amminoacidi non modifica le concentrazioni di acido lattico nel sangue, né migliora la resa atletica quando l’intensità dell’esercizio è elevata, il che significa che vengono bruciati prevalentemente zuccheri e quindi l’integrazione è superflua.
Tuttavia, vi sono evidenze che la somministrazione di aminoacidi ramificati possa essere utile all’atleta durante esercizi prolungati ad intensità moderate che producano concentrazioni di acido lattico inferiori alla cosiddetta soglia di attività aerobica (quando cioè l’acido lattico prodotto è in equilibrio con quello demolito). Ciò viene spiegato con il fatto che, al diminuire della concentrazione sanguigna degli aminoacidi ramificati (segno che essi vengono degradati) aumentano i livelli di un altro aminoacido, il triptofano. Esso compete con gli aminoacidi ramificati nella fuoriuscita dai capillari negli spazi intercellulari, ed entra in contatto con il tessuto nervoso del cervello. Qui il triptofano viene trasformato in serotonina, che induce sensazioni di stanchezza mentale e sonnolenza. Se i livelli di triptofano sono più elevati di quelli degli aminoacidi ramificati, l’atleta sentirà prima la stanchezza, ma se vengono somministrate integrazioni di aminoacidi ramificati la stanchezza tarderà a farsi sentire.
Ci sono anche sempre maggiori evidenze sperimentali che gli aminoacidi ramificati forniti in supplemento facilitino la ripresa fisica dopo l’esercizio. Infatti, dato che essi entrano nella regolazione del metabolismo proteico nel muscolo, se somministrati in supplemento la loro degradazione eviterà che vengano intaccate le proteine muscolari, con conseguenti minori danni ai tessuti.
Link
http://www.sinu.it/larn/proteine.asp#AMINOACIDI� ; Societ� italiana di nutrizione umana
http://www.albanesi.it/Alimentazione/amino.htm
http://www.albanesi.it/Alimentazione/aminoacidi.htm
http://en.wikibooks.org/wiki/Biochemistry_-_Proteins_-_The_chemistry_of_proteins
http://www.nonsolofitness.it/argomenti/alimentazione.asp?sez=25
http://mips.gsf.de Munich information center for protein sequences, una banca dati sulla sequenza delle proteine
Bibliografia
Dohm et al., 1977. Adaptations to endurance training at three intensities of exercise. J Appl Physiol. 42: 753-757.
Lemon, Mullin, 1980. Effect of initial muscle glycogen levels on protein catabolism during exercis Journal of Applied Physiology, 48(4): 624-629.
Kasperek and Snider, 1987. Effect of exercise intensity and starvation on activation of branched-chain keto acid dehydrogenase by exercise. Am J Physiol Endocrinol Metab 252:33-37.
Wagenmakers, 1991. L�Carnitine supplementation and performance. In: Brouns, F. (ed.): Advances in nutrition and top sport. Karger, Basel 32 (1991) pp. 110�127.
Van Hall, Raaymakers, Saris, Wagenmakers, 1994. Supplementation with branched-chain amino acids (BCAA) and tryptophan has no effect on performance during prolonged exercise. Clin Sci. 87: 52.