Caro Riccardo,
un anglosassone direbbe oggi che la regola dell'ottetto "is just a useful bookkeeping system": senz'altro utile per predire il numero di legami che un dato elemento può formare con altri atomi all'interno di una molecola, ma niente più di quello. In effetti la regola dell'ottetto non ha particolari basi chimico-fisiche o, almeno, per come viene riportata in molti testi, razionalizzata e giustificata non è neppure molto corretta, e non spiega nulla.
Un elettrone è una particella subatomica piuttosto particolare: è talmente piccola che ha qualità fisiche sia particellari che di onda. Heisenberg, nel 1927, dimostrò che il suo moto intorno al nucleo non consente di poter determinare contemporaneamente la sua posizione precisa nello spazio e la sua esatta velocità. Per questa ragione i chimici hanno individuato determinate regioni dove le probabilità di trovare l’elettrone orbitante sono piuttosto alte, dell’ordine del 90%. Dobbiamo ringraziare Schrödinger se conosciamo la forma di questi orbitali: infatti introdusse un’equazione matematica detta “funzione d’onda” che, grazie a tre parametri denominati n, l ed m, stabilisce in che regione di spazio intorno al nucleo si colloca l’elettrone.
Se potessimo vedere ad occhio nudo un atomo, esso ci apparirebbe come una tenue nube tremolante dai contorni sfumati, esattamente come in questa immagine artistica:

Atomo ed orbitali annessi
Il parametro n è detto numero quantico principale, assume valori interi positivi (1, 2, 3…) ed indica il livello energetico dell’orbitale. Più l’orbitale è lontano dal nucleo, più l’energia negli elettroni dovrà essere alta per potervi orbitare intorno. Tale energia, a scale così piccole, può avere solo quantità ben definite dette “pacchetti quantici”. Quindi gli elettroni si troveranno solo a determinate distanze dal nucleo.
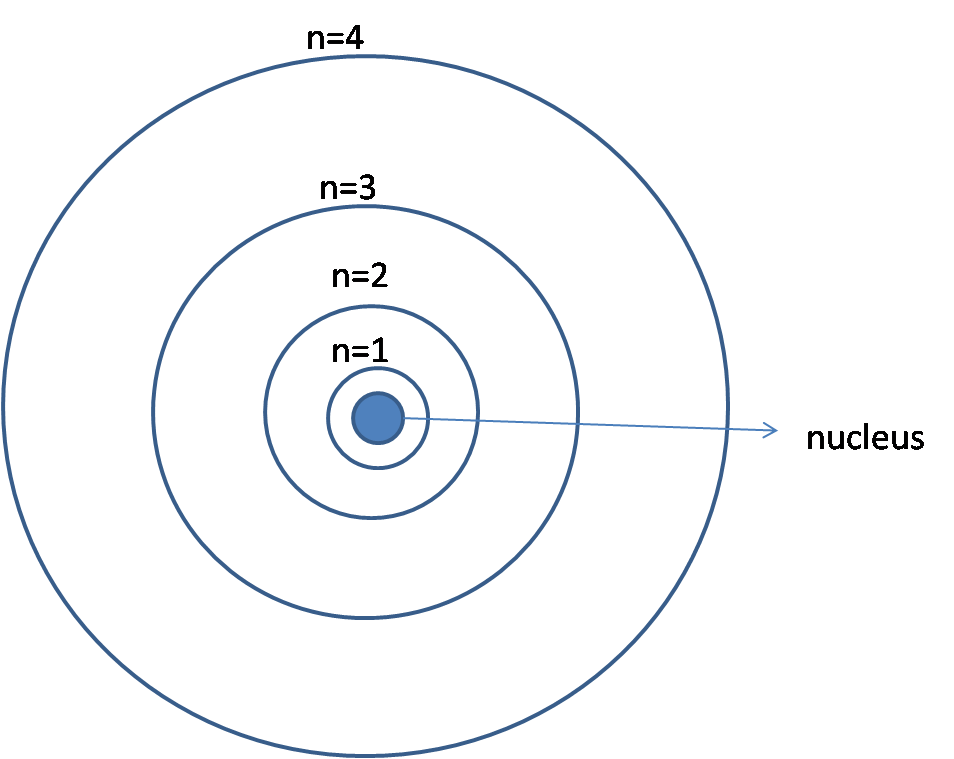
Livelli energetici definiti dal numero quantico principale n. Si notino le distanze crescenti dal nucleo dell’atomo.
Il parametro l invece è il numero quantico azimutale, assume valori fra 0 ed n-1 e definisce che forma deve avere l’orbitale. Tali valori di l sono denominati sottolivelli, e sono indicati con la lettere s (sharp), p (principal), d (diffuse), f (fundamental). Questi primi due numeri definiscono l’energia complessiva dell’orbitale. Le forme di s, p, d ed f sono mostrate nella seguente figura.
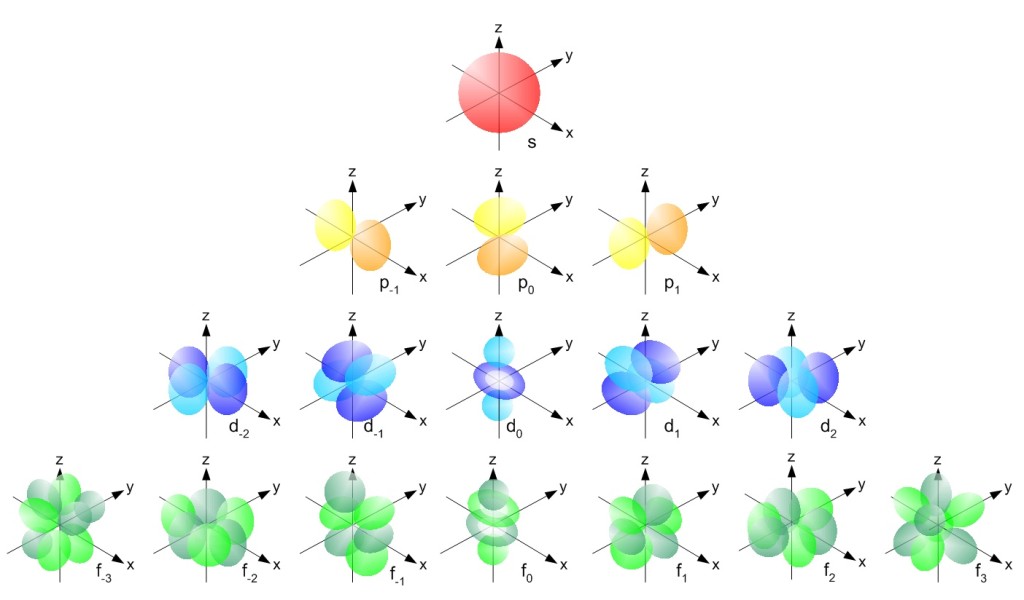
Forme di orbitale definite dal parametro l e orientate secondo il numero quantico m, esse sono la rappresentazione dello spazio in cui orbitano gli elettroni
Il numero quantico m, che assume valori fra –l ed l, definisce l’orientamento dell’orbitale nello spazio, l’orientamento degli orbitali è ben visibile nella figura precedente (0 per s; -1, +1 per p; -2, +2 per d; -3, +3 per f).
Esiste anche un quarto numero quantico che indica in quale direzione l’elettrone ruota su se stesso, ed è detto di spin.
Fatta questa complessa ma doverosa introduzione, bisogna dire che ogni livello energetico può contenere fino a un massimo di otto elettroni accoppiati fra loro in un orbitale. Inizialmente gli elettroni occuperanno tutti orbitali diversi dello stesso sottolivello energetico (s, p, d o f per intenderci): gli elettroni nel livello energetico più esterno occuperanno prima gli orbitali vuoti disponibili, finendo per orbitare da soli in questi ultimi, tali elettroni sono detti spaiati; i successivi invece dovranno condividere uno degli orbitali già occupati con un altro elettrone e così via, fino ad avere il riempimento degli orbitali del sottolivello energetico considerato.
Soltanto il livello energetico più interno può contenere al massimo una sola coppia di elettroni, mentre i livelli immediatamente superiori, da n=2 in poi per intenderci, potranno ospitare fino a un massimo di otto elettroni.
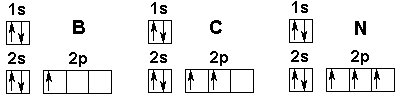
Configurazione elettronica degli atomi di boro (B), carbonio (C), e azoto (N). Il livello energetico 1 è tutto occupato da due elettroni; il secondo livello energetico presenta due sottolivelli: s e p. Il sottolivello s è pieno; il sottolivello p invece si riempie a mano a mano che aumenta il numero di elettroni. Gli orbitali, in questo schema, sono rappresentati dai quadrati, le frecce sono invece rappresentano gli elettroni che li occupano. La punta indica la direzione di rotazione dell’elettrone. Si può notare come gli elettroni tendano ad occupare prima gli orbitali vuoti del sottolivello 2p, ma già partendo dall’elemento successivo all’azoto, ossia l’ossigeno, una coppia di elettroni sarà costretta a condividere un orbitale di 2p.
La regola dell’ottetto nasce da questo tipo di configurazione elettronica.
Un atomo infatti, per essere stabile, deve avere una configurazione orbitale quanto più stabile possibile: se l’orbitale esterno dell’atomo ha un solo elettrone, esso tenderà a cederlo per trovare l’equilibrio energetico. E’ il caso del sodio, che cede l’unico elettrone del suo livello energetico più esterno al cloro. Al cloro infatti ne manca uno per completare il suo livello energetico più esterno: infatti in esso orbitano sette elettroni. Una volta che il sodio cede l’elettrone al cloro, esso assume carica positiva, mentre il secondo carica negativa; i due ioni si attraggono e si uniscono formando così un legame ionico.
C’è ad esempio l’ossigeno che, nel suo livello energetico più esterno, ha sei elettroni orbitanti: quattro occupano due orbitali totalmente pieni, e altri due invece orbitano nei restanti orbitali che risultano semivuoti. L’ossigeno potrà allora condividere gli orbitali semivuoti con due atomi di idrogeno che hanno anch’essi un solo elettrone nel loro orbitale. Tale condivisione di elettroni consente a entrambi gli atomi di poter completare i loro sottolivelli energetici, raggiungendo così la stabilità energetica. In questo modo si ha una condivisione di orbitali che crea un legame detto covalente. Altro esempio di legame covalente sono due atomi di idrogeno che condividono i loro elettroni per completare il loro orbitale.
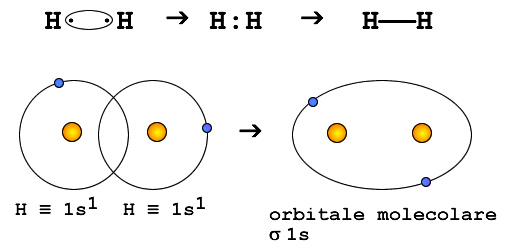
Legame covalente fra due atomi di idrogeno
Esistono anche atomi che non si legano ad altri elementi, in quanto il loro livello energetico più esterno ha otto elettroni ed è quindi completo. E’ il caso dei gas nobili come il neon, il cripton, l’argon, il radon e lo xeno. Sono definiti nobili proprio per questa loro caratteristica di elementi inerti, dovuta all’assenza di esigenza di completamento o dal non bisogno di cessione di elettroni isolati, come accade invece per sodio, calcio, potassio, rubidio, litio, francio o cesio, caratterizzati dalla presenza di un unico elettrone nel loro livello energetico più esterno e di cui devono disfarsi, divenendo così ioni positivi.
Il fine di tutto è trovare la stabilità energetica: un atomo dal livello energetico più esterno incompleto è instabile: un elettrone spaiato che vaga lontano dal resto della nube elettronica infatti è facilmente catturabile da un atomo di passaggio che deve completare il suo livello energetico più esterno. Tali interrelazioni sono anche favorite da geometrie orbitali piuttosto articolate e complesse, che portano gli elettroni spaiati ad arrivare in regioni estremamente lontane dello spazio intorno al nucleo.
Si conclude che è la configurazione elettronica a decidere il carattere interattivo di un atomo con un altro atomo e quindi il suo modo di interagire. In tutto questo la regola dell’ottetto è un riferimento pratico che consente di comprendere quale può essere la strategia adottata da quest’ultimo, sia essa l’inerzia, o la creazione di un legame covalente o ionico.