HNF1-β, conosciuto anche con il nome di LB3 o vHNF1, è un fattore di trascrizione nucleare inizialmente ritrovato a livello degli epatociti (HNF=hepatocyte nuclear factor). È un fattore di trascrizione, cioè una proteina regolativa composta da un dominio di legame al DNA, che riconosce una corta sequenza di DNA ci circa 10 coppie di basi e da un dominio di attivazione o di repressione che influisce sulla trascrizione genica.
In particolare HNF1-β, descritto come la variante di HNF1 (v-HNF), è costituito da un dominio POU atipico, un omeodominio divergente e un dominio di dimerizzazione all’N-terminale.
Questo fattore di trascrizione non è ristretto agli epatociti, come farebbe presupporre il nome, ma in queste cellule è stato trovato per la prima volta a livelli elevati anche nell’adulto. La sua espressione durante lo sviluppo è strettamente correlata a quella di HNF1-1α e si presenta pressoché invariato in tutte le specie di Vertebrati finora esaminati. L’espressione di vHNF1 precede quella di HNF1 durante l’embriogenesi e la sua mutazione è letale in stadi molto precoci, almeno nel topo. I tessuti principali, il cui sviluppo è regolato da vHNF1, sono il tessuto extraembrionale, l’endoderma e conseguentemente il mesoderma. Proprio l’importanza di vHNF1 nel tessuto extraembrionale spiega il motivo di una letalità così elevata della sua mutazione. Un vHNF1 mutato, infatti, porta ad una errata organizzazione di questo tessuto, dal quale deriveranno gran parte degli annessi indispensabile per la sopravvivenza dell’embrione.
Per quanto riguarda endoderma e mesoderma, l’espressione precoce di vHNF1 in questi siti è stata provata per numerose specie, tra le quali Xenopus laevis e topo. vHNF1 è stato ormai definito come un marcatore precoce del differenziamento dell’endoderma e delle strutture che da esso derivano, quali fegato, rene e pancreas. È stato ipotizzato che una delle varianti del diabete giovanile sia causato proprio da una mutazione in vHNF1.
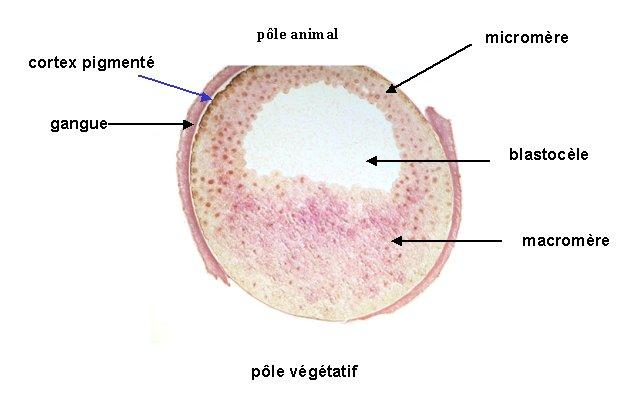
In Xenopus, ad esempio, il primo sito di espressione si trova a livello del polo vegetativo della blastula, una regione cruciale per l’insorgenza dei segnali induttivi per il mesoderma. Da questo emisfero derivano poi le cellule endodermiche, le quali continuano ad esprimere questo fattore.
Studi successivi hanno portato all’ipotesi, ormai ampiamente accreditata, che questa proteina sia un fattore permissivo più che istruttivo e che debba quindi essere associato con altre molecole segnale a funzione induttiva sulla formazione delle strutture meso-endodermiche. A seconda dell’organo preso in considerazione, ovviamente, queste molecole variano, essendo per lo più tessuto-specifiche.
Un’ultima considerazione riguarda l’esistenza, provata nell’embrione di topo, di due isoforme derivate da splicing alternativo: vHNF1A e vHNF1B. Riguardo alla differenza nei ruoli di queste due isoforme durante lo sviluppo, si conosce ancora molto poco ma è certo che vHNF1A è predominante e si presuppone che il rapporto quantitativo tra vHNF1A e vHNF1B possa svolgere un ruolo nella differenziazione tissutale.
Ecco alcuni lavori al riguardo:
– Haumaitre C, Reber M, Cereghini S. Functions of HNF1 family members in differentiation of the visceral endoderm cell lineage. J Biol Chem 2003 Oct 278:40933-42
– Vignali R, Poggi L, Madeddu F, Barsacchi G HNF1(beta) is required for mesoderm induction in the Xenopus embryo. Development 2000 Apr 127:1455-65
– Coffinier C, Gresh L, Fiette L, Tronche F, Schütz G, Babinet C, Pontoglio M, Yaniv M, Barra J- Bile system morphogenesis defects and liver dysfunction upon targeted deletion of HNF1beta. Development 2002 Apr 129:1829-38
– Demartis A, Maffei M, Vignali R, Barsacchi G, De Simone V. Cloning and developmental expression of LFB3/HNF1 beta transcription factor in Xenopus laevis. Mech Dev 1994 Jul 47:19-28
Blastula