Ogni nucleo è
caratterizzato da un numero di massa, indicato dalla
lettera A, e da un numero atomico indicato dalla
lettera Z.
Il numero Z
rappresenta il numero di protoni, mentre il numero di
massa A rappresenta il numero totale di nucleoni
cioè la somma del numero Z di protoni e del
numero N di neutroni che costituiscono il nucleo.
Cioè:
A
= Z + N
Nuclei che hanno lo
stesso valore di Z ma diversi valori di A si chiamano isotopi.
In altre parole gli isotopi sono nuclei che hanno lo
stesso numero di protoni ma diverso numero di neutroni.
Nel nucleo protoni e
neutroni sono soggetti alla forza nucleare che li tiene
legati fortemente insieme.
Se gli A nucleoni che
costituiscono il nucleo interagissero tra loro solamente
tramite la forza elettromagnetica, il nucleo si
disintegrerebbe, dato che la forza agente sarebbe quella
repulsiva tra i protoni (che hanno la stessa carica
elettrica). Ciò significa che, almeno a distanze
inferiori a 3·10-15 m, le forze
nucleari sono molto più intense di quelle coulombiane
(vedi figura).
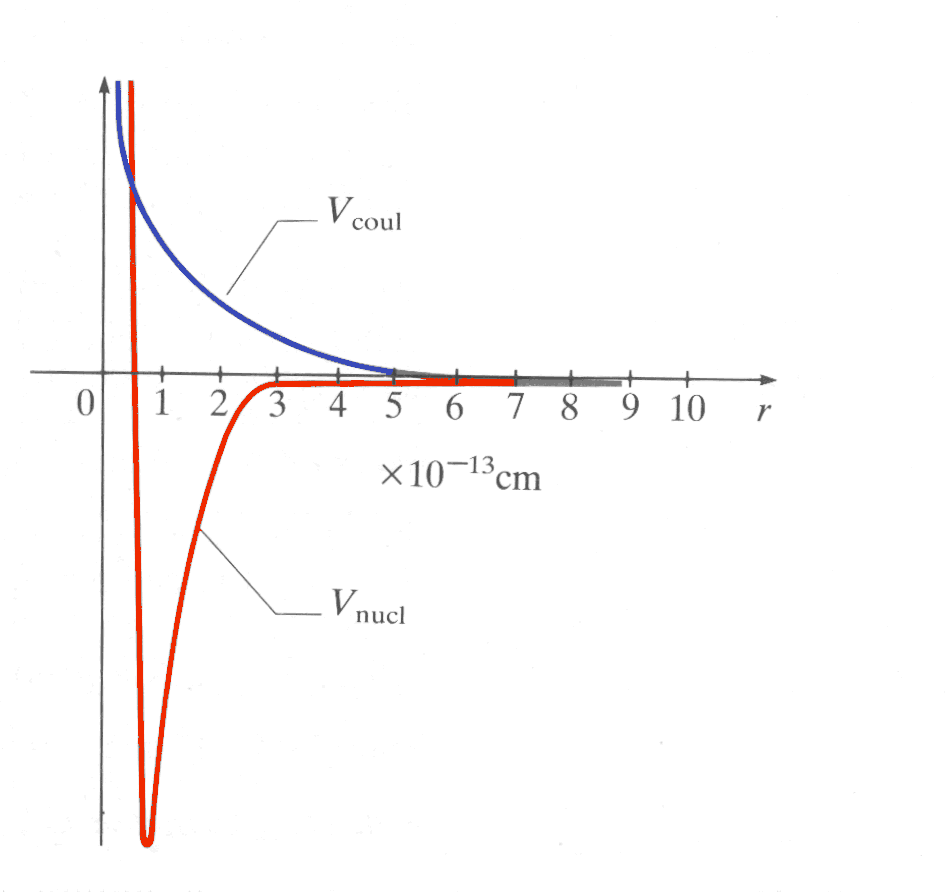
La forza nucleare può
essere caratterizzata dalle seguenti proprietà:
- è una forza
conservativa; - è nulla per
distanze superiori a 3,0 ·10-15 m,
mentre diventa fortemente attrattiva per distanze
inferiori; - è fortemente
repulsiva a distanze molto piccole (inferiori a
0,5·10-15 m);
Misurando la massa di un
nucleo e confrontandola con la somma delle masse dei
nucleoni che lo costituiscono, scopriamo un fatto
apparentemente strano: quando protoni e neutroni sono
legati in un nucleo, hanno una massa minore rispetto a
quando sono separati.
Consideriamo, per
esempio, il nucleo del deuterio che è un isotopo pesante
dell’idrogeno, costituito da un protone e da un
neutrone. Esso ha massa:
MD
= 3,3434 ·10-27 Kg
mentre la somma delle
masse di un protone e di un neutrone è uguale a:
Mp
+ Mn = ( 1,6725·10-27 +
1,6748·10-27) Kg = 3,3473 ·10-27
Kg
Se calcoliamo la
differenza tra la somma delle masse del protone e del
neutrone liberi (Mp + Mn)
e la massa del deuterio (MD) otteniamo:
DM
= (Mp + Mn) – MD
= (3,3473·10-27 – 3,3434 ·10-27) Kg
= 0,0039 ·10-27 Kg
cioè 0,0039 ·10-27
Kg di massa sono scomparsi (difetto di massa).
Poiché sappiamo che
massa ed energia sono equivalenti si può pensare che la
massa mancante si sia trasformata in energia secondo la
relazione
E
= mc2 (1)
Immaginiamo di costruire
il deuterio avvicinando un protone ed un neutrone.
Quando, a distanze molto piccole, entrano in gioco le
forze attrattive nucleari, dobbiamo frenare le due
particelle compiendo un lavoro negativo. In altri termini
la formazione del deuterio riversa energia
nell’ambiente circostante. In particolare, ogni
volta che si forma il deuterio, sono liberati fotoni
gamma di energia pari a 2,22 MeV (milioni di
elettronvolt).
Dalla relazione (1)
ricavando la massa si ha:
![]()
energia che è uguale
alla massa scomparsa.
Il difetto di massa di
un nucleo corrisponde, pertanto, all’energia
liberata durante la sua formazione.
Il prodotto del difetto
di massa per il quadrato della velocità c della luce nel
vuoto è, quindi, uguale all’energia di legame del
nucleo, cioè all’energia che occorre fornire al
nucleo per separare i nucleoni e portarli molto lontani
gli uni dagli altri.