22-05-2005
per
commenti
osservazioni
critiche
e ringraziamenti
![]()
scrivi all'autore
buongiorno, vorrei sapere come si può produrre del fenolo in laboratorio, partendo dal benzene. Se sì,quale ruolo prenderebbe un eventuale catalizzatore nella reazione.
la ringrazio anticipatamente.
Speri Enrico
(risponde Raffaele Ricco)
- Breve storia e sintesi industriale del fenolo
Il fenolo è uno tra i più semplici derivati del benzene e il capostipite della classe che da esso prende il nome. Ha formula C6H5OH, è un solido cristallino bianco dal caratteristico odore. Fu scoperto da Runge nel 1934 nel catrame di carbon fossile; pochi anni dopo Lister ne riconobbe le proprietà antisettiche e ne consigliò l’uso prima degli interventi chirurgici. Sebbene non venga praticamente più impiegato a questo scopo e sia stato soppiantato da prodotti meno caustici e tossici, è tuttora prodotto e molto usato per produrre plastiche, coloranti e farmaci. Nell' industria, il fenolo viene convenientemente preparato passando attraverso la formazione di un intermedio, il cumene o isopropilbenzene, partendo da benzene e propilene tramite una normale reazione di sostituzione elettrofila aromatica (in questo caso si tratta di un’alchilazione di Friedel-Crafts) catalizzata da un acido di Lewis quale l’alluminio tricloruro o l’acido fosforico, più economico del precedente e quindi industrialmente preferito; la reazione viene normalmente condotta in fase gassosa, a 250°C e alla pressione di 30 atmosfere. Il meccanismo è il seguente:
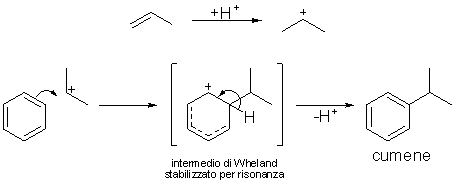
Lo stadio successivo prevede l’ossidazione del cumene da parte dell’ossigeno dell’aria in presenza di quantità catalitiche di iniziatore radicalico (benzoil perossido, ad esempio) ed in condizioni lievemente basiche (i doppietti elettronici sono stati omessi per chiarezza):
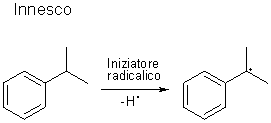
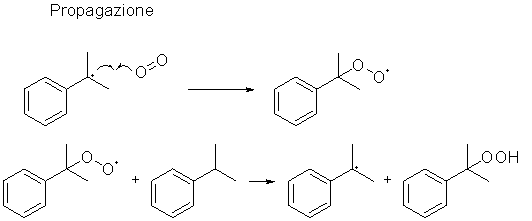
Il cumene idroperossido viene quindi idrolizzato in ambiente acido per dare fenolo e acetone, tramite trasposizione dell’intermedio che si forma:
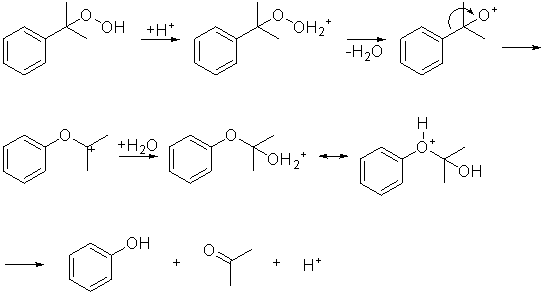
La maggior parte del fenolo e dell’acetone viene usata nella sintesi del bisfenolo A, un monomero base per la produzione di resine epossidiche e plastiche al policarbonato (CD, vetri di sicurezza, lenti per occhiali da sole, rivestimenti, contenitori per liquidi e cibi, ecc…)
- Sintesi di laboratorio
Sebbene il database Beilstein di chimica organica riporti svariate procedure (se ne contano poco più di 80) per la conversione del benzene a fenolo in un unico stadio, in laboratorio il fenolo non viene ottenuto direttamente da questo, a meno di non dover preparare dei derivati particolari. E’ possibile applicare in laboratorio la sintesi del fenolo dal cumene, che in questo caso è preparato per alchilazione del benzene con n-propil cloruro in presenza di alluminio tricloruro. L’uso di un alogenuro lineare è previsto in quanto si forma comunque il carbocatione secondario, più stabile (per effetto iperconiugativo):

La sintesi più comune del fenolo in laboratorio viene comunque fatta per diazotazione dall’anilina. Per produrre quest’ultima, si nitra il benzene con una miscela di acido nitrico e acido solforico, quindi si riduce con stagno (o ferro) e acido cloridrico, oppure per idrogenazione catalitica, o ancora usando idruri metallici. Di seguito è presentato uno schema dei due passaggi:
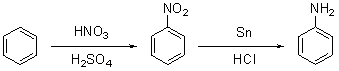
Queste sono tipiche procedure per la produzione di nitrobenzene (1) e anilina (2) in laboratorio (NOTA: le quantità sono state omesse per ragioni di sicurezza, e si sconsiglia di provare tali procedure se non adottando le dovute precauzioni e soprattutto avvalendosi di personale competente):
1) In un pallone munito di termometro viene posto acido nitrico concentrato, si raffredda in un bagno d’acqua e ghiaccio e si aggiunge acido solforico concentrato a piccole porzioni e sotto agitazione. Si introduce il benzene a piccole porzioni, evitando che la temperatura superi i 55°. Al termine dell’aggiunta, si monta un refrigerante a ricadere e si scalda a 60°C per 40-45 minuti. Al termine, si versa tutto con cautela in acqua fredda, agitando in modo che il nitrobenzene venga lavato bene dai residui acidi. Si lascia separare le fasi (il nitrobenzene, essendo più denso, rimane sul fondo) e si elimina la fase acquosa acida superiore. Si trasferisce il nitrobenzene in un imbuto separatore e si lava con acqua. Si essicca il nitrobenzene su cloruro di calcio anidro e si filtra. Il liquido viene quindi distillato raccogliendo la frazione che bolle tra 206 e 211 °C; ottenendo così un liquido giallo pallido e trasparente. Non bisogna superare i 214°C né distillare a secchezza in quanto il residuo, composto da prodotti di nitrazione superiore, può esplodere. Si ricorda che il nitrobenzene è tossico.
2) In un pallone munito di refrigerante a ricadere viene posto il nitrobenzene precedentemente preparato e stagno in granuli. Dal condensatore viene aggiunto con estrema cautela acido cloridrico concentrato a piccole porzioni: la miscela diventerà rapidamente calda, ed occorre raffreddare il pallone prima di ogni successiva aggiunta e mai se la miscela è troppo calda o inizia a bollire. Terminata l’aggiunta si scalda a 100°C per 30-60 minuti. A temperatura ambiente, si aggiunge cautamente una soluzione di idrossido di sodio in di acqua evitando di portare a ebollizione la miscela. Si distilla in corrente di vapore raccogliendo solo la coda. A causa della seppur bassa solubilità dell’anilina in acqua, essa dev’essere “strippata” per salatura. Il distillato così saturato viene estratto in imbuto separatore con etere dietilico e la fase organica essiccata con carbonato di potassio anidro (il calcio cloruro non può essere impiegato perché reagisce con l’anilina). Dopo aver filtrato via il solido, si rimuove l’etere per distillazione oppure usando un evaporatore rotante, quindi si distilla l’anilina raccogliendo la frazione tra 180 e 184 °C. Anche l’anilina è tossica.
L’anilina così prodotta viene sottoposta alla reazione di diazotazione, processo molto versatile per produrre una grande varietà di composti:
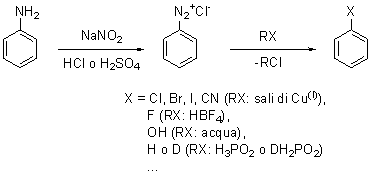
In questo caso, si usa un nitrito (comunemente di sodio) e acido cloridrico o acido solforico a bassa temperatura; un meccanismo – molto semplificato – comunemente accettato (poiché non ancora completamente compreso a fondo) è il seguente:
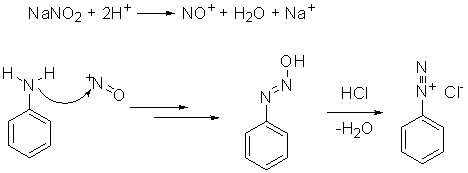
Successivamente, riscaldando il sale di diazonio in acqua si ottiene il fenolo:
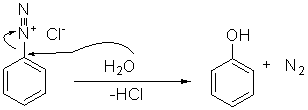
Una procedura tipica è la seguente:
In un pallone si pone acqua e acido solforico concentrato (mai viceversa), e anilina, riscaldando se necessario per facilitarne la dissoluzione. Si aggiunge acqua fredda e si pone in un bagno di ghiaccio, in modo che la temperatura scenda al di sotto dei 5°C e agitando vigorosamente per separare l’anilina solfato in cristalli finemente suddivisi. Si aggiunge lentamente una soluzione acquosa di nitrito di sodio: il solfato di anilina si discioglie rapidamente durante la reazione. Per determinare la fine della reazione si può prendere una goccia di miscela e farla reagire con una soluzione di ioduro di potassio, quindi aggiungere della salda d’amido: se la soluzione diventa nera la diazotazione è completa. Si lascia reagire per 15-20 minuti, quindi si scalda a 50°C per circa 15 minuti, o comunque finché cessa l’evoluzione di azoto. Si distilla in corrente di vapore e si “strippa” via l’acqua come visto precedentemente, estraendo poi con etere e seccando su potassio carbonato o magnesio solfato anidri. Si distilla quindi il fenolo raccogliendo la frazione tra 179 e 183 °C. Il fenolo fonde a 43°C, quindi per raffreddamento cristallizza nel recipiente di raccolta. Il fenolo ha azione corrosiva sulla pelle e sulle mucose.
La strada così percorsa che porta da benzene a fenolo, nonostante richieda tre passaggi, viene comunemente usata per la produzione di derivati del benzene anche complessi, variando in modo opportuno le condizioni di lavoro, poiché si utilizzano processi relativamente semplici e facilmente scalabili, con reagenti economici, stabili e largamente disponibili, e arrivando a rese di reazione più che soddisfacenti.
Ci sono altri due importanti metodi indiretti di preparazione del fenolo:
a) si passa attraverso la sintesi dell’acido benzensolfonico, usando benzene e oleum, ovvero anidride solforica disciolta in acido solforico concentrato. L’acido benzensolfonico viene quindi sottoposto a fusione alcalina con sodio idrossido ad alta temperatura:
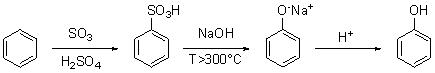
b) un metodo applicabile anche industrialmente (processo Raschig-Hooker) prevede la fusione alcalina del clorobenzene in condizioni analoghe al metodo precedente. Il clorobenzene si sintetizza da benzene e cloro, usando un acido di Lewis quale ferro tricloruro come catalizzatore; si può anche usare direttamente ferro e formare il catalizzatore in situ:
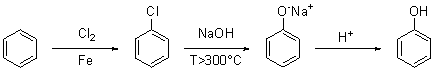
---
Fonti:
- Practical Organic Chemistry, Vogel
- Chimica Organica, Baker & Engel
- Wikipedia (http://en.wikipedia.org)